Formacion de Compuestos Quimicos Inorganicos
| Sitio: | 'ELE' Plataforma Educativa Chaqueña |
| Área temática: | Ciencias Naturales: Química |
| Libro: | Formacion de Compuestos Quimicos Inorganicos |
| Imprimido por: | Invitado |
| Día: | viernes, 5 de junio de 2026, 04:41 |
Descripción
en este libro tendrán como se forman todos los FCQI
1. Compuestos Quimicos
Compuestos Químicos
Los elementos naturales se combinan de diferentes modos para formar casi tres millones de sustancias compuestas que se conocen en la actualidad y reciben la denominación genérica de compuestos químicos ó simplemente, compuestos.
Estos compuestos se clasificaron en inorgánicos y orgánicos.
Los compuestos orgánicos solo podrían ser elaborados por los seres vivos, luego se comprobó que esto no era cierto, y fueron sintetizados en el laboratorio- sin la intervención de los seres vivos. Pero esta clasificación se mantuvo para facilitar el estudio del elevado número de compuestos existentes.
.VALENCIA
El número de átomos de cada uno de los elementos que intervienen en la formación de un compuesto depende de los electrones que necesitan Ganar ó Perder para adquirir la configuración electrónica del gas inerte más próximo. Por esta razón los elementos presentan diferente capacidad para combinarse unos con otros. Esta capacidad de combinación recibe el nombre de VALENCIA del elemento químico.
ELECTROVALENCIA
Los METALES procuran ceder e- de su órbita más externa, mientras que los NO METALES tratan de ganar e- para completar el octeto.
Entonces en las uniones iónicas el Nro. de Valencia de los elementos está dado por el Nro. de e- que ceden o que ganan al establecer la unión. Esta Valencia recibe el nombre de ELECTROVALENCIA
COVALENCIA
En las combinaciones entre no metales se pueden establece diferentes uniones covalentes, (como ya vimos). Entonces en éste tipo de uniones –covalentes- el Nro de Valencia de los elementos depende del Nro. de e- que comparten éste tipo de Valencia se denomina COVALENCIA.
El número de VALENCIA de un elemento está dado por el número de electrones que el átomo cede, gana ó comparte en una Unión Química
Representación de las valencias y fórmulas estructurales o desarrolladas
Para representarla Valencia de los elementos en las uniones iónicas y covalentes, se escribe el símbolo del elemento y rodeado por guiones, tantos como sea su Nro. de Valencia.
| ||
Na- Cl- -Ca- -O- -Al- -C- =N-
| | |
Entonces ahora se puede representar gráficamente la unión entre los átomos por medio de las denominadas fórmulas estructurada


1.1. ¿COMO SE CLASIFICAN LOS COMPUESTOS QUÍMICOS?
Pueden estar formados por 2, 3, 4 ó mas elementos, esto le permite clasificarlos en Binarios, Ternarios, Cuaternarios, etc.
COMPUESTOS BINARIOS
Estos compuestos están formados por dos elementos químicos, entre ellos se encuentran:
1) Óxidos 2) Hidruros
3) Sales de Hidrácidos
2. ¿Qué son Los Óxidos?
Son compuestos BINARIOS (dos elementos) formados por OXIGENO y otro elemento químico:
a) Si ese otro elemento químico es un NO METAL se denomina Óxido Ácido.
b) Si ese otro elemento químico es un METAL se denomina Oxido Básico.
“como el oxigeno es un elemento muy abundante y reactivo, existen grandes cantidad de óxidos en la Naturaleza”
2.1. Oxidos Basicos
ÓXIDOS BÁSICOS
Son Compuestos Binarios que resultan de la combinación un METAL mas OXÍGENO

para observar el desarrollo de como se forman los Óxidos Básicos realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito.
2.2. Óxidos Ácidos o Anhídridos
ÓXIDOS ÁCIDOS Ó ANHÍDRIDOS
Son Compuestos Binarios que resultan de la combinación de un NO METAL mas OXÍGENO

para observar el desarrollo de como se forman los Óxidos Ácidos o Anhídridos realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito.
3. HIDRUROS
Son compuestos binarios que
resultan de la combinación del Hidrogeno que trabaja con valencia 1 y forman hidruros Metálicos al combinarse con un METAL ; y al combinarse con un NO METAL forman Hidruros No Metalices
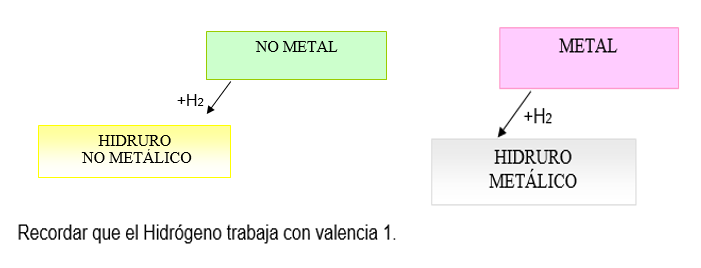
3.1. Hidruros Metalicos
Son compuestos binarios que resultan de la combinación de un METAL más HIDRÓGENO.
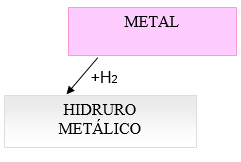
para observar el desarrollo de como se forman los Hidruros Metálicos realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito.
3.2. Hidruros No Metálicos
Son compuestos binarios que resultan de la combinación de un NO METAL más HIDRÓGENO.
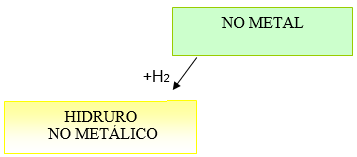
Recordar que el Hidrógeno trabaja con valencia 1
para observar el desarrollo de como se forman los Hidruros NO Metálicos realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito.
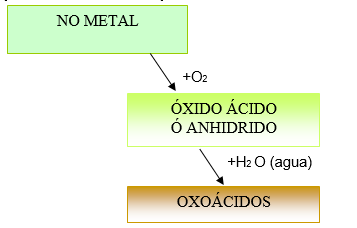
4. OXÁCIDOS U OXOACIDOS
Son compuestos TERNARIOS que resultan de la combinación de ANHÍDRIDO con H2O.
![]()
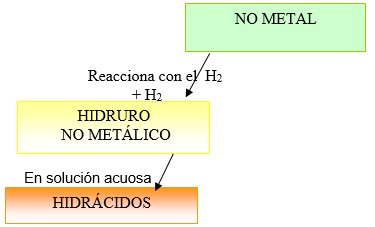
5. HIDRACIDOS
Son compuestos BINARIOS más
específicamente son cinco ( 5 ) hidruros NO METALES (actúan con la menor
valencia); que al disolverse en agua H2O adquieren propiedades
similares a los Ácidos , ellos son:
![]() Fluoruro
de H2 HF
Fluoruro
de H2 HF
Cloruro de H2 HCl
Bromuro de H2 HBr Hidruros en estado puro (gases)
Yoduro de H2 HI
Sulfuro d H2 H2S la menor valencia de S es 2 por ello aparece el subíndice 2.
Cuando están en solución acuosa: se comportan como ácidos y reciben el nombre de Hidrácidos:
HF ( en solución acuosa ) se llama Ácido FluorHídrico.
HCl (en solución acuosa) se llama Ácido Clorhídrico.
HBr ( en solución acuosa) se llama Ácido BromHídrico.
HI (en solución acuosa) se llama Ácido IodHídrico
H2S (en solución acuosa) se llama Ácido SulfHídrico
6. HIDROXIDOS O BASES O ÁLCALIS
Son compuestos TERNARIOS ( 3 Elementos ) que
resultan de la combinación de “ un óxido básico + H2O “. Se
caracteriza por representa el radical Oxidrilo
ó Hidroxilo . Este radical está constituido por un átomo de O y otro de H, unido fuertemente entre sí y
actuando como si fuera un solo átomo y el radical ( OH ) presenta valencia
igual a uno

para observar el desarrollo de como se forman los HIDROXIDOS O BASES realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito.
7. DISOCIACION IONICA de ÁCIDOS e HIDROXIDOS
Los oxácidos son compuestos que al disolverse en H2O se disocian en iones o sea que se “ioniza”. Este proceso se llama disociación iónica.
EXPLICACIÓN:
Como el H2O es una molécula polar, tiene un polo ( + ) y un polo ( - ); tiende a romper las uniones de los ácidos y disociarlos en H+ (catión Hidrógeno) = (protón) y el anión restante. El átomo de Hidrógeno perdió su electrón y quedo como H+ =(protón) y el resto de la molécula se quedo con ese electrón por eso se convierte en (anión)-.
REGLA GENERAL:
Catión = Carga Positiva, Ej: Protón = H+
Anión = Carga Negativa
NOMENCLATURA: Cuando el
ácido termina en OSO el anión correspondiente cambia el sufijo a (ITO); y
cuando el ácido termina en ICO el anión termina en (ATO).
Regla Nemotécnica: “pICO de pATO … OSO chiquITO”

para observar el desarrollo de como se forman LA DISOCIACION IONICA EN AGUA realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito
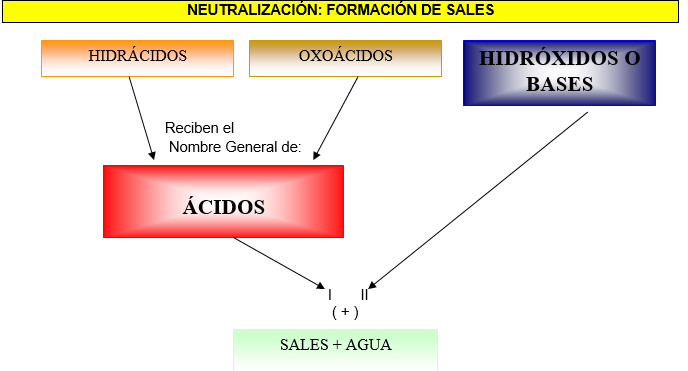
8. NEUTRALIZACION: FORMACION DE SALES
Cuando a una solución de un hidróxido, en la que se encuentran Cationes y Aniones OXHIDRILOS , se le añade una “Solución Ácida” que contiene PROTONES y ANIONES, se produce una Reacción Química en la que: el anión (OH)- del Hidróxido se une al Protón del Ácido formando una molécula de H2 O; y el “catión” del Hidróxido se une con el “anión” del ácido formando una SAL + H2O
para observar el desarrollo de como se forman LA NEUTRALIZACION :FORMACION DE SALES realicen un clic aquí; luego resolver las actividades y subirlas en el lugar de tareas; hasta lueguito