LEY DE LOS GASES IDEALES
2. LEYES
LEY DE LOS GASES IDEALES
Los gases ideales es una simplificación de los gases reales que se realiza para estudiarlos de manera más sencilla. En sí es un gas hipotético que considera:
- Formado por partículas puntuales sin efectos electromagnéticos.
- Las colisiones entre las moléculas y entre las moléculas y las paredes es de tipo elástica, es decir, se conserva el momento y la energía cinética.
- La energía cinética es directamente proporcional a la temperatura.
- Los gases se aproximan a un gas ideal cuando son un gas mono atómico, está a presión y temperatura ambiente.
La ecuación del gas ideal se basa condensa la ley de Boyle, la de Gay-Lussac, la de Charles y la ley de Avogadro.
Ley de Avogadro
Esta ley relaciona la cantidad de gas (n, en moles) con su volumen en litros (L), considerando que la presión y la temperatura permanecen constantes (no varían).
El enunciado de la ley dice que:
El volumen de un gas es directamente proporcional a la cantidad del mismo.
Esto significa que:
ü Si aumentamos la cantidad de gas, aumentará el volumen del mismo.
ü Si disminuimos la cantidad de gas, disminuirá el volumen del mismo.
Esto tan simple, podemos expresarlo en términos matemáticos con la siguiente fórmula:
![]()
que se traduce en que si dividimos el volumen de un gas por el número de moles que lo conforman obtendremos un valor constante.

Esto debido a que si ponemos más moles (cantidad de moléculas) de un gas en un recipiente tendremos, obviamente, más gas (más volumen), así de simple.
Esto se expresa en la ecuación
![]() simplificada es
simplificada es ![]()
Veamos un ejemplo práctico y sencillo:
Tenemos 3,50 L de un gas que, sabemos, corresponde a 0,875 mol. Inyectamos gas al recipiente hasta llegar a 1,40 mol, ¿cuál será el nuevo volumen del gas? (la temperatura y la presión las mantenemos constantes).
Solución:
Aplicamos la ecuación de la ley de Avogadro:
![]()
y reemplazamos los valores correspondientes:
![]()
resolvemos la ecuación, multiplicando en forma cruzada:
![]()
Ahora, despejamos V 2 , para ello, pasamos completo a la izquierda el miembro con la incógnita (V 2 ), y hacemos:
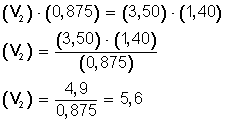
Respuesta:
El nuevo volumen (V 2 ), ya que aumentamos los moles hasta 1,40 (n 2 ), es ahora 5,6 L
Observar el Video explicativo haciendo clic en el siguiente enlace.

Ley de Boyle-Mariotte
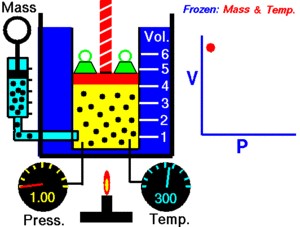
Ley de Boyle
Esta ley nos permite
relacionar la presión y el volumen de un gas
cuando la temperatura es constante.
La ley de Boyle
(conocida también como de Boyle y Mariotte) establece que la presión de
un gas en un recipiente cerrado es inversamente proporcional al
volumen del recipiente, cuando
la temperatura es constante.
Lo cual significa que:
ü El volumen de un gas es inversamente proporcional a la presión que se le aplica:
En otras palabras:
ü Si la presión aumenta, el volumen disminuye.
ü Si la presión disminuye, el volumen aumenta.
Esto nos conduce a que, si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
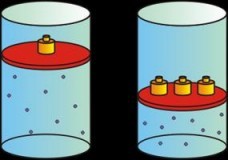
Matemáticamente esto es: P . V= k
lo cual significa que el producto de la presión por el volumen es constante.
Para aclarar el concepto:
Tenemos un cierto volumen de gas (V 1 ) que se encuentra a una presión P 1 . Si variamos la presión a P 2 , el volumen de gas variará hasta un nuevo valor V 2 , y se cumplirá:
P 1 V 1 = P 2 V 2 .
que es otra manera de expresar la ley de Boyle.
Apliquemos la fórmula en un ejemplo práctico:
Tenemos 4 L de un gas que están a 600 mmHg de presión. ¿Cuál será su volumen si aumentamos la presión hasta 800 mmHg? La temperatura es constante, no varía.
Solución:
Como los datos de presión están ambos en milímetros de mercurio (mmHg) no es necesario hacer la conversión a atmósferas (atm). Si solo uno de ellos estuviera en mmHg y el otro en atm, habría que dejar los dos en atm.
Aclarado esto, sustituimos los valores en la ecuación P 1 V 1 = P 2 V 2 .

Si bien la Ley de Charles es una ley que nos indica la relación que existe entre el volumen y la temperatura, (tomar en cuenta esto), nos da a conocer un simple y sencillo razonamiento, que nos parecerá obvio.
Si nosotros ponemos un recipiente con gas en una estufa, y a ese recipiente lo sometemos a cierta temperatura, ¿Qué pasará con el recipiente con gas?, ¿Sufrirá algún cambio?, pues bien, para darle respuesta a esto es muy importante saber que la Ley de Charles, nos dice lo siguiente:
Al someter cierta masa de gas a presión constante y la temperatura en aumento, el volumen aumentará, y al disminuir la temperatura, también el volumen disminuirá
Si la presión es constante entonces de la ley general en estado gaseoso tendrá el siguiente cambio:
Dónde:
T1 = Temperatura inicial
T2 = Temperatura final
V1 = Volumen inicial
V2 = Volumen final
¡Muy importante! La temperatura la vamos a medir en grados Kelvin
Fórmula de la Ley de Charles
En resumen, la fórmula que utilizaremos para resolver problemas de la ley de Charles, será entonces:
El volumen puede estar expresado en centímetros cúbicos, metros cúbicos e incluso litros. Depende del autor del problema. A diferencia de la temperatura que siempre debe ser expresada de forma absoluta, es decir en grados Kelvin.
Ley de Charles Gráfica
La gráfica es muy importante para entender este tema.
Notables científicos, físicos y químicos dedicaron parte de su tiempo para poder entender mejor esta ley, pero fue Gay-Lussac un físico-químico de origen francés, que estudió a fondo el comportamiento de los gases respecto a la relación entre la presión y la temperatura, su ley estable lo siguiente.
la Ley de Gay-Lussac dice: Si el volumen de una masa gaseosa permanece constante, la presión es directamente proporcional a su temperatura absoluta.
Fórmula de Gay-Lussac
Como dijimos texto atrás, la proporcionalidad que existe en esta ley es
sobre la presión y la temperatura, matemáticamente colocaremos esto como:
Ahora introduzcamos una constante de proporcionalidad esto da paso a que se
vea de la siguiente forma, es como un despeje simple.
Ahora al tratarse de una igualdad, podemos
considerar las condiciones inicial y final, quedando la
ecuación o fórmula matemática de la Ley de Gay-Lussac de la siguiente forma: donde
P1= Presión inicial T1=Temperatura Inicial P2= Presión Final T2=Temperatura Final
Gráfica de la Ley de Gay-Lussac
En la gráfica podremos observar claramente la proporcionalidad entre la presión y la temperatura, recordemos también que para las condiciones de un gas, las temperaturas deben darse en grados Kelvin.